9 <<< pag.10 >>> 11



 2 minuti con ...
2 minuti con ...
il prof. Marcello Buiatti
NADiRinforma: nel corso della V edizione del Festival Evocamondi La mia acqua, la mia Terra abbiamo incontrato il prof. Marcello Buiatti, professore ordinario di Genetica all'Università di Firenze. In perfetto parallelismo con il lavoro scientifico il professore collabora con il gruppo di filosofia della Biologia chiudendo un cerchio di conoscenze che riescono a rendere esaustivi e comprensibili i processi dinamici della vita.
Produzione Arcoiris Bologna
Visita il sito: http://www.evocamondi.it

 Evocamondi 2008:
Evocamondi 2008:
intervento del prof. Marcello Buiatti
NADiRinforma propone l'intervento del prof. Marcello Buiatti al Festivale Evocamondi La mia Acqua, la mia Terra organizzato dall'Assoc. Temporale tenutosi a Bentivoglio (bo) il 21 giugno 2008. Il prof. Buiatti è docente di genetica all'Università di Pisa, i suoi interessi sono numerosi, ma si concentrano soprattutto sullo studio dei processi dinamici della vita. Contemporaneamente al lavoro scientifico collabora da molti anni con gruppi di filosofia della biologia ed ha scritto numerosi saggi sull'evoluzione dei concetti biologici in particolare dalla seconda metà dell'ottocento ad oggi, sulle interazioni fra le comunità scientifiche e la società e i loro effetti sullo spirito del tempo. Buiatti, in qualità di presidente dell'associazione ambientalista Environment and Work e della Fondazione Toscana sostenibile si occupa di sicurezza, di politiche di sostenibilità, di educazione ambientale.
Facciamo luce sugli Ogm
mercoledì 14 novembre 2007
di MARCELLO BUIATTI
professore ordinario di Genetica
Università di Firenze
Nonostante i molti tentativi di condurre il dibattito sugli OGM a una discussione razionale sui problemi reali, purtroppo il nostro Paese, ormai abituato, ahimé, più a fare il tifo sulle parole che a ragionare sulle cose, continua a dividersi su argomenti ormai vecchi confondendo la gente in modo colpevole. Innanzitutto tutti sembrano credere che i prodotti delle cosiddette biotecnologie siano moltissimi e vari e frutto di una tecnologia molto avanzata che ha già dato grandi risultati. Questo è falso: in questomomento oltre cento milioni di ettari sono coltivati ad OGM ma questi appartengono solo a tre tipi,piante resistenti ad insetti, a diserbanti o a tutti e due.
Le piante OGM in commercio sono solo quattro e cioè soia, mais, cotone e colza ma gran parte delle coltivazioni sono delle prime due specie e il numero delle varietà modificate è addirittura risibile se lo si confronta con quello delle piante prodotte dalla rivoluzione verde, frutto del miglioramento genetico tradizionale, in cui moltissimi caratteri furono migliorati e decine di migliaia di nuove linee create. Il fatto è che la tecnologia che è stata usata per gli OGM oggi coltivati è vecchia di venti anni, e in questo periodo niente di nuovo è entrato sul mercato nonostante la enorme spesa per la ricerca e i tantissimi OGM presenti nei laboratori. L'ultimo dei tanti fallimenti è stato il cosiddetto Golden Rice, contenente un gene per la provitamina A, presentato come la salvezza dalle carenze vitaminiche per i popoli del Sud del Mondo. Dopo un impressionante battage pubblicitario questo prodotto è stato ritirato dal mercato perché la quantità di vitamina che produceva era nettamente inferiore al fabbisogno.
Ogm, verità e falsi miti
L'intervento di Marcello Buiatti, professore ordinario di Genetica all'Università di Firenze
La ragione di questo fallimento è molto semplice. Chi, come me, è del mestiere, sa che quando mettiamo un frammento di DNA in una pianta non sappiamo a priori quante copie entrano nel suo patrimonio genetico, dove si inseriscono, se si modificano, come interagiscono con la rete della pianta e con la sua fisiologia. In tuttii casi, tolti i due che infatti sono sul mercato, la introduzione di un gene proveniente da un organismo molto diverso modifica negativamente il fine equilibrio nella rete dei geni dell'individuo ricevente formatosi durante la evoluzione. Questo porta ad effetti non previsti della modificazione e a scarsa produttività della pianta. Se ne sono rese conto anche le grandi multinazionali che ora fanno molto meno ricerca su piante ad uso alimentare e invece stanno costruendo piante produttrici di farmaci e di sostanze ad uso industriale. Intendiamoci bene, la presenza di effetti imprevisti non significa necessariamente un aumento del rischio per la nostra salute.Tanto per sgombrare il campo da un altro equivoco, bisogna chiarire qui che i prodotti ora in commercio non risultano essere particolarmente pericolosi per la salute. L'unico pericolo, che purtroppo non viene mai nominato nelle accese discussioni su questo argomento, viene dal fatto che le piante resistenti ai diserbanti permettono di fare trattamenti fino alla epoca del raccolto con il rischio che ci sia ancora diserbante nel cibo che poi mangiamo. Potrebbero invece essere pericolose le piante che producono farmaci, se allevate in pieno campo perché potremmo assumerli senza averne bisogno e lo stesso vale per quelle che danno sostanze aduso industriale. Il rischio quindi, non viene dalla tecnica di per sé stessa, ma va valutato per ogni singolo prodotto e spesso dipende dall'uso del prodotto stesso, come nel caso della resistenza a diserbanti. Ed è infatti proprio dall'uso degli OGM che vengono i veri problemi. Gli OGM che sono sul mercato sono fatti per un'agricoltura industriale su larga scala, certo non biologica dato che comportano l'uso dei diserbanti, ma nemmeno di qualità perché puntano ad avere piccoli guadagni su larghe estensioni tutte coltivate con lo stesso materiale, come avviene negli Stati Uniti, ma anche in Brasile dove ci sono aziende di centomila ettari e oltre. Contrariamente a quello che si pensa, inoltre, la modificazione genetica non ha portato ad un aumento della resa per ettaro e questo dato si ricava da una fonte non sospetta, il Dipartimento della Agricoltura USA.Guardando infatti i dati in un periodo che va dai primi anni 80 in cui non c'erano OGM ad oggi con il 90% coltivato ad OGM , la produzione di soia per ettaro è rimasta costante e quella del mais è aumentata ma con la stessa velocità durante tutto il periodo dimostrando che l'aumento è dovuto al miglioramento genetico tradizionale e non si è accelerato con l'introduzione di OGM. Gli OGM, quind,i nel nostro Paese, con aziende di ridotta o ridottissima dimensione e senza praticamente aumento di produzione non ci servono e anzi sono dannosi perché non sono voluti dai consumatori che invece chiedono una agricoltura di qualità, basata su prodotti sicuri, diversificati per venire incontro alla varietà dei cibi su cui sono basate le nostre agricolture (il plurale non è a caso). Non li vorrebbero nemmeno i popoli del Sud del Mondo che sono però stati costrettia coltivarli per il debito contratto con gli USA come è successo in Brasile dove per coltivare soia che viene poi tutta esportata al Nord del Mondo e usata come mangime, sono state cacciate le famiglie contadine e distrutte le agricolture locali. Queste sono le vere e giuste ragioni per cui laToscana insieme con l'Alta Austria ha dato inizio alla rete delle Regioni libere da OGM che ormai comprende oltre quaranta aderenti. Su questo è importante ragionare seriamente, mantenendosi razionalmente vigili sul problema del rischio senza inutili paure e pensando invece a quale modello di vita, di società, di economia, di agricoltura, vogliamo puntare nel futuro. (Marcello Buiatti) (tratto da: Dimensione Agricoltura)

SICUREZZA DEI PRODOTTI ALIMENTARI
TEMI SPECIFICI
Alcune questioni rivestono un'importanza particolare per i cittadini, soprattutto se sono legate alla loro salute. L'Unione europea agisce in questi settori per prevenire e eliminare i rischi, ad esempio in materia di organismi geneticamente modificati, o nel caso di determinate malattie che colpiscono gli animali, come le encefalopatie spongiformi bovine o l'afta epizootica.
ORGANISMI GENETICAMENTE MODIFICATI (OGM)
-
Introduzione OGM
-
Alimenti e mangimi geneticamente modificati
-
Nuovo regolamento concernente la tracciabilità e l'etichettatura di organismi geneticamente modificati (OGM)
-
Identificatori unici degli OGM
-
Emissione di organismi geneticamente modificati
-
Impiego confinato di microrganismi geneticamente modificati
-
Movimenti transfrontalieri degli organismi geneticamente modificati
ENCEFALOPATE SPONGIFORMI TRASMISSIBILI (EST) E BOVINE (ESB)
-
Prevenzione, controllo e eradicazione delle EST
-
EST: nuovo punto della situazione
-
Misure legate all'alimentazione animale:
AFTA EPIZOOTICA
-
Lotta contro la febbre aftosa
-
Soppressione della vaccinazione preventiva ()
Organismo geneticamente modificato
Da Wikipedia, l'enciclopedia libera.
Un organismo geneticamente modificato (OGM) è un essere vivente che possiede un patrimonio genetico modificato tramite tecniche di ingegneria genetica che consentono l'aggiunta, l'eliminazione o la modifica di elementi genici.
Definizione di OGM
Nonostante le modificazioni ed il trasferimento di materiale genetico avvengano in natura in molteplici occasioni e tali processi "naturali" siano all'origine della diversità della vita sulla terra, con il termine Organismo Geneticamente Modificato si intende solamente un individuo le cui modificazioni genetiche siano state operate dall'uomo attraverso moderne tecniche di ingegneria genetica.
Gli OGM vengono spesso indicati come organismi transgenici : l'associazione tra i due termini è imprecisa: infatti si parla di transgenesi esclusivamente nel caso di inserimento di geni esogeni all'interno di un dato organismo, mentre risultano essere OGM anche quegli organismi la cui modifica non prevede l'inserimento di materiale genetico esterno. Ad esempio inserendo un gene di banano in un banano con le tecniche del DNA ricombinante si genera un OGM cisgenico ; viceversa inserendo ad esempio il gene di un animale o di un batterio in un vegetale si ha un OGM transgenico . Stesso discorso per l'eliminazione, tramite tecniche di biologia molecolare, di un frammento di DNA dal genoma di un organismo.
Tecniche principali
Ai fini della definizione di OGM data dalla Direttiva 2001/18/CE, sono considerate tecniche che hanno come risultato un organismo geneticamente modificato:
tecniche di ricombinazione del materiale genetico che comportano la formazione di nuove combinazioni mediante inserimento in un vettore di molecole di DNA , RNA o loro derivati, nonché il loro inserimento in un organismo ospite nel quale non compaiono per natura, ma nel quale possono replicarsi in maniera continua;
-
tecniche che comportano l'introduzione diretta in un organismo di materiale ereditabile preparato al suo esterno, tra cui la microiniezione, la macroiniezione e il microincapsulamento;
-
fusione cellulare (inclusa la fusione di protoplasti) o tecniche di ibridazione per la costruzione di cellule vive, che presentano nuove combinazioni di materiale genetico ereditabile, mediante la fusione di due o più cellule, utilizzando metodi non naturali.
Sono esclusi dalla definizione gli organismi ottenuti per mutagenesi o fusione cellulare di cellule vegetali di organismi che possono scambiare materiale genetico anche con metodi di riproduzione tradizionali, a condizione che non comportino l'impiego di molecole di acido nucleico ricombinante.
Miglioramento genetico tradizionale ed ingegneria genetica
La modificazione del genoma è stata operata per secoli, prima dell'avvento dell' ingegneria genetica , tramite diverse tecniche. Una delle tecniche di modifica del DNA che sta alla base della selezione (sia naturale che operata dall'uomo) è la mutazione casuale, un fenomeno che è presente in tutti gli esseri viventi, anche se a una frequenza molto bassa. Tale frequenza può essere aumentata dall'esposizione a radiazioni o a agenti chimici mutageni.
Le mutazioni hanno portato nel tempo ad evidenti modifiche geniche - non solo attraverso mutazioni puntiformi (ossia riferite a brevissimi tratti di cromosoma o a singoli nucleotidi ), ma anche attraverso delezioni e traslocazioni di intere regioni cromosomiche - che nei secoli hanno permesso all'uomo di costituire e selezionare molte varietà agrarie e popolazioni animali oggi utilizzate nel comparto agro-alimentare.
Un esempio storico di mutazioni indotte dall'uomo ai fini del miglioramento genetico è rappresentato dalla varietà di frumento " Creso ", ottenuto per irradiazione dall' ENEA . Esso è stato negli anni ottanta una delle varietà di punta per la produzione di pasta (circa 1 spaghetto su 4) ed è oggi uno dei genitori delle attuali varietà commerciali [2] .
Un'altra tecnica di miglioramento genetico molto diffusa è l'incrocio, non solo tra individui della stessa specie, ma tra specie per le quali è possibile riscontrare una compatibilità riproduttiva o per le quali è comunque possibile rimuoverne le barriere. In tal modo si sono prodotti il mulo o il bardotto , ma anche gli ibridi oggi utilizzati per le produzioni animali e vegetali. Il vantaggio di tale tecnica è la possibilità, una volta identificata fenotipicamente una caratteristica di interesse in una specie (ad esempio la resistenza ad una malattia), di trasferirla in un'altra attraverso incroci mirati.
La differenza sostanziale tra le tecniche di miglioramento genetico tradizionale e l'ingegneria genetica (alla base dello sviluppo degli OGM) sta nella predittività dei risultati. Nel caso della mutazione o dell'incrocio viene effettuata una selezione fenotipica , in base a caratteristiche visibili, all'interno di popolazioni molto grandi (alcune decine di migliaia nelle piante e alcune centinaia negli animali). Ultimamente si sta sempre più affermando nel campo del miglioramento genetico da incrocio l'impiego dei marcatori biochimici e molecolari i quali permettono di semplificare notevolmente i tempi e le modalità di lavoro poiché non rendono necessaria l'espressione fenotipica del carattere di interesse nella progenie. A differenza della mutagenesi, in cui i geni che conferiscono un determinato carattere sono indotti artificialmente e le caratteristiche sono acquisite grazie a mutazioni casuali del genoma, nell'ingegneria genetica si "progetta" la modifica da effettuare sapendo esattamente l'obbiettivo da perseguire e le modalità con cui perseguirlo. Una volta ottenuto un certo numero di organismi geneticamente modificati si selezionano genotipicamente , ovvero in base alle caratteristiche genetiche, gli individui che presentano le caratteristiche desiderate e che quindi risultano più idonei al progetto.
Storia
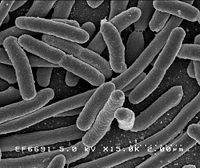 Immagine al microscopio elettronico a scansione di E.coli , il primo batterio modificato tramite tecniche di ingegneria genetica
Immagine al microscopio elettronico a scansione di E.coli , il primo batterio modificato tramite tecniche di ingegneria genetica
Il primo OGM moderno fu ottenuto nel 1973 da Stanley Cohen (Stanford University School of Medicine ) e Herbert Boyer ( University of California, San Francisco). I due ricercatori, grazie all'uso combinato delle nuove tecniche di biologia molecolare che si stavano sviluppando in diversi laboratori, come l'uso dell' enzima ligasi (1967), degli enzimi di restrizione e della trasformazione batterica (1970 - 72), riuscirono per primi a clonare un gene di rana all'interno del batterio Escherichia coli , dimostrando che era possibile trasferire materiale genetico da un organismo ad un altro tramite l'utilizzo di vettori plasmidici in grado di autoreplicarsi, abbattendo di fatto le barriere specie-specifiche [3] [4] .
Questi risultati ebbero un tale impatto da indurre la comunità scientifica ad autoimporre nel 1974 una moratoria internazionale sull'uso della tecnica del DNA ricombinante per valutare la nuova tecnologia ed i suoi possibili rischi. Quello stesso anno fu la Conferenza di Asilomar , tenutasi a Pacific Grove ( California ) [5] [6] a concludere che gli esperimenti sul DNA ricombinante potessero procedere a patto che rispettassero severe linee guida, poi redatte dai National Institutes of Health (NIH) ed accettate dalla comunità scientifica. Queste linee guida, pubblicate per la prima volta nel 1976 [7] e successivamente aggiornate, sono tuttora seguite dai laboratori che effettuano esperimenti di trasformazione genica [8] .
Dal 1976 ad oggi gli OGM sono passati dallo stato di mera possibilità tecnologica ad una realtà. Si sono dovuti attendere infatti solo due anni da Asilomar per avere il primo prodotto ad uso commerciale derivato da un OGM. La Genentech , fondata da Herbert Boyer, è riuscita infatti a produrre attraverso E. coli importanti proteine umane ricombinanti: la somatostatina ( 1977 ) e l' insulina ( 1978 ), il farmaco biotecnologico più noto, che è stato commercializzato a partire dal 1981 [9] . La commercializzazione dell'insulina ha segnato un cambiamento epocale per l'industria del farmaco, aprendo il settore biotecnologico (precedentemente confinato nei laboratori di ricerca) all'industrializzazione, e rivoluzionando il processo di drug discovery e lo sviluppo di nuove terapie non invasive.
Poco dopo lo sviluppo dell'insulina ricombinante, nel 1983 si ebbe negli Stati Uniti la prima battaglia sul rilascio nell'ambiente di organismi geneticamente modificati. Al centro del dibattito la sperimentazione dei cosiddetti batteri ice-minus , una variante di Pseudomonas syringae incapace di produrre la proteina di superficie che facilita la formazione dei cristalli di ghiaccio . I ricercatori della Advanced Genetic Sciencies e della University of California, Berkeley svilupparono questa variante allo scopo di introdurla nel terreno per proteggere le piante dal gelo. La richiesta di effettuare esperimenti in campo aperto con questo OGM scatenò una forte contestazione da parte degli ambientalisti. Solo dopo una battaglia legale durata tre anni, nel 1986 i batteri ice-minus furono i primi OGM ad uscire dai laboratori ed essere introdotti nell'ambiente. Pochi anni dopo si scoprì che questa variante esisteva anche in natura e l'azienda detentrice del brevetto, visto il contesto non favorevole agli OGM, decise di proseguire gli esperimenti solo sulla variante naturale. Gli ice-minus ricombinanti non vennero mai commercializzati [10] .
Dopo più di 30 anni dalla Conferenza di Asilomar, all'alba del XXI secolo si conoscono molte delle potenzialità e dei limiti di questa tecnologia e, in molti casi, si dispone dei protocolli di gestione necessari a consentirne una applicazione in sicurezza. In particolare il Protocollo di Cartagena , ratificato nel 2000 , si pone come strumento internazionale per la protezione della biodiversità dai possibili rischi derivanti dalla diffusione dei prodotti delle nuove tecnologie.
Ad oggi la tecnica del DNA ricombinante è stata utilizzata non solo per la produzione di nuovi farmaci, ma anche di enzimi per ridurre l'impatto ambientale dell'industria, piante e animali con caratteristiche migliorative in termini di resistenza alla malattie o di performance produttive e ambientali, ma anche organismi quali l' oncotopo , usato nella ricerca sul cancro , che hanno portato con sé importanti quesiti etici oltre ad aver aperto la strada a dispute per l'uso a fini sperimentali o commerciali delle innovazioni scientifiche [11] . La possibilità di brevettare gli OGM ha acceso un forte dibattito sulla proprietà intellettuale delle risorse genetiche del pianeta e sulla liceità di una ricerca e di un'industria che non si ponga anche dei limiti etici o che non sappia mettersi in ascolto delle domande presenti nell'opinione pubblica creando consenso attorno alle proprie iniziative di ricerca e business .
Applicazioni
Gli OGM sono oggi utilizzati nell'ambito dell' alimentazione , dell' agricoltura , della medicina , della ricerca, e dell' industria .
Agricoltura |
Alimentazione |
Medicina |
Industria |
|
Batteri |
|
|
|
|
Miceti |
|
|
||
Piante |
|
|
|
|
Animali |
|
|||
Produzione di OGM
 Animazione della struttura a doppia elica del DNA.
Animazione della struttura a doppia elica del DNA.
Le tecniche per ottenere gli OGM sono relativamente recenti. Oggi sono presenti sul mercato unicamente OGM che presentano modifiche circoscritte a caratteri di natura mendeliana , ovvero caratteri facilmente controllabili tramite l'inserimento di uno o pochi geni che servono a fornire direttamente una data caratteristica (es. resistenza a una malattia). L'esponenziale aumento di informazioni rese disponibili nell'ultimo decennio dalla genomica consente però di mettere a punto organismi che presentino modifiche genetiche molto complesse su caratteri quantitativi (es. resistenza agli stress, produzione).
Gli OGM vengono ottenuti attraverso l'uso di tecniche di ingegneria genetica che permettono di inserire, all'interno del genoma di un organismo, frammenti di DNA provenienti anche da altri organismi. Il DNA così ottenuto è definito DNA ricombinante . I frammenti di DNA da inserire vengono estratti dal genoma di origine attraverso l'uso di enzimi di restrizione , che funzionano come vere e proprie forbici molecolari, e inseriti in un vettore ricevente grazie ad un altro enzima: la DNA ligasi . I vettori possono essere sia piccole molecole circolari di DNA, i plasmidi che possono accogliere frammenti fino a circa 15.000 paia di basi , sia alcune strutture derivate da virus , in grado di contenere quantità maggiori di materiale genetico (fino a circa 70.000). Esistono inoltre vettori che rappresentano dei veri e propri cromosomi artificiali ad esempio in lievito (noti come YAC , dall'inglese Yeast Artificial Chromosomes ) o in batteri ( BAC , Bacterial Artificial Chromosomes ) che permettono l'inserimento di oltre 300.000 paia di basi - cioè oltre lo 0,01% del genoma di un mammifero.
Classi di OGM
Procarioti
Per inserire nuovi frammenti di DNA negli organismi si usano dei " vettori ". I vettori sono generalmente piccole molecole circolari di DNA, i plasmidi , o strutture derivate da virus in grado di immagazzinare materiale genetico.
Sono tre i processi attraverso cui è possibile modificare il genoma batterico
La trasformazione batterica è un processo, osservabile in natura, attraverso il quale alcuni procarioti (detti competenti ) sono in grado di ricevere del DNA esterno in grado di produrre nuove caratteristiche di fenotipo . Questo fenomeno fu scoperto nel 1928 da Frederick Griffith ma venne confermato solo nel 1944 . La biologia molecolare si è servita dei batteri competenti per studiarne i meccanismi. Oggi sono state sviluppate alcune tecniche, per quanto molto empiriche, in grado di rendere competenti anche batteri che non lo sono naturalmente. È stato dimostrato, infatti, che l'ingresso di DNA è ampiamente facilitato dalla presenza di certi cationi , come Ca 2+ , o dall'applicazione di una corrente elettrica (tecnica detta della elettroporazione ). I vettori utilizzati nelle trasformazioni sono essenzialmente plasmidi: in seguito all'ingresso, i plasmidi non si integrano nel genoma, ma rimangono autonomi (in uno stato detto episomale ).
Nella coniugazione batterica , il DNA è trasferito da un batterio all'altro attraverso un pilum (concettualmente un tubo che può collegare per breve tempo i due batteri). Un plasmide può essere così trasferito da un organismo all'altro. La coniugazione, molto frequente in natura, è poco sfruttata come tecnica di modificazione genetica.
La trasduzione è infine l'inserimento di materiale genetico nel batterio attraverso un virus batteriofago .
Per inserire il segmento di DNA che codifichi il gene voluto, è necessario conoscere la funzione dei geni su cui si sta operando. Nei batteri, è relativamente semplice identificare la funzione di un gene specifico: i ricercatori a tale scopo sono soliti realizzare dei ceppi batterici cosiddetti knock out . In questi ceppi viene eliminato il DNA relativo al gene d'interesse: osservando le conseguenze sulla vita del batterio, è possibile identificare la funzione del gene stesso.
L'uso di knock out è molto diffuso, non solo per i procarioti. È possibile realizzare knock out in numerosi organismi modello . Il gene responsabile della fibrosi cistica , ad esempio, è stato individuato in topi knock-out : una volta individuato il presunto gene della fibrosi cistica (chiamato CFTR ) nell'uomo, i ricercatori hanno individuato l'omologo nel genoma del topo, ne hanno fatto un knock out verificando poi che senza tale gene il topo presentava tutti i sintomi clinici della malattia.
Piante
(Per approfondire, vedi la voce Piante transgeniche)
L a scorticatura su una radice generata da Agrobacterium tumefaciens
a scorticatura su una radice generata da Agrobacterium tumefaciens
La principale tecnica di modificazione genetica per le piante è legata alla capacità naturale del batterio Agrobacterium tumefaciens di infettare piante e causare una crescita paragonabile a quella tumorale presente negli animali, tale patologia è nota come "galla del colletto". A. tumefaciens è in grado di infettare la pianta trasferendo un plasmide che è in grado di integrarsi nel genoma dell'ospite. Il plasmide contiene diversi geni che, una volta "letti" dalla pianta, generano la galla e producono nutrienti per il batterio consentendone la crescita. Diversi scienziati, a partire dalla seconda metà degli anni sessanta, hanno contribuito a comprendere il meccanismo e le condizioni attraverso cui tale plasmide viene trasferito ed integrato nel genoma della pianta: tra questi Jeff Schell, Marc Van Montagu, Georges Morel, Mary-Dell Chilton e Jacques Tempé. Grazie a tali scoperte, a partire dal 1983 è stato possibile trasformare le conoscenze biologiche acquisite, in tecniche biotecnologiche e quindi sviluppare versioni del plasmide "disarmate", ovvero senza i geni che davano origine alla malattia, in cui erano invece presenti geni di interesse, permettendo così di produrre le prime piante transgeniche , oggi molto utilizzate per fini di ricerca o agro-alimentari.
Un altro processo largamente utilizzato per produrre piante OGM è il metodo biolistico (anche detto gene gun o particle gun ), che permette di "sparare" microproiettili ricoperti di DNA all'interno delle cellule vegetali. Tale metodo è stato utilizzato, ad esempio, per la produzione del più comune cereale OGM, il Mon810 .
Le tecniche biolistiche sono spesso utilizzate per piante monocotiledoni , mentre A.tumefaciens ed altri agrobatteri sono utilizzati per modificare dicotiledoni , anche se recentemente sono stati messi a punto ceppi di questo batterio in grado di trasformare anche le monocotiledoni.
Queste tecniche sono in generale complementari e non sostitutive di quelle, più empiriche, già sviluppate all'interno del millenario processo di "umanizzazione" delle piante di interesse agro-alimentare che oggi si trovano sulle nostre tavole: il loro patrimonio genetico ha infatti subito nel corso del tempo modifiche genetiche rilevanti con tecniche convenzionali (oppure, si potrebbe dire, biotecnologie classiche ), che hanno dato origine alla stessa agricoltura : selezione artificiale o, più recentemente, l'induzione di mutazioni per mezzo di raggi X o raggi gamma .
Animali
Diverse tecniche sono utilizzate per la produzione di animali transgenici. Il primo esperimento di successo di transgenesi animale fu ottenuto utilizzando un retrovirus [12] . Questa tecnica si ispira a un fenomeno che avviene in natura: durante le infezioni virali, l' RNA dei retrovirus entra nella cellula dell'animale infetto, viene modificato in DNA e integrato nel genoma dell'ospite. Questa proprietà fa del retrovirus un buon vettore per materiale genetico, anche se questa tecnica presenta alcune limitazioni. Altri esperimenti hanno usato cellule staminali embrionali o germinali, ma il trasferimento nucleare (la tecnica utilizzata per la produzione della pecora Dolly ) associato alla manipolazione in vitro di colture cellulari è attualmente la tecnica più in uso [13] .
Gli scopi principali della transgenesi animale sono i seguenti:
Produzione di biomedicine . Sebbene la produzione di biomolecole da parte di batteri o lieviti sia più economica, queste tecniche presentano alcuni limiti dovuti alle differenze metaboliche delle cellule batteriche rispetto a quelle animali. Per questo motivo si è sviluppato un grande interesse per lo sfruttamento di tecniche di transgenesi per far produrre agli animali grandi quantità di molecole utilizzabili in terapia e prevenzione, quali farmaci , anticorpi o vaccini . La produzione di biomolecole può avvenire attraverso diversi liquidi biologici, di cui quello di più facile sfruttamento sarebbe il latte, che viene prodotto in grandissime quantità. Tra le biomolecole prodotte da animali transgenici già ad uno stadio avanzato di sviluppo (alcune già in fase di approvazione per la vendita negli Stati Uniti ) ci sono anticorpi policlonali e lattoferrina prodotti da bovini, fattore antitrombina III prodotto da capre e calcitonina prodotta da coniglie. Alcuni effetti non desiderati sono tuttavia stati riscontrati a volte negli animali impiegati a questi scopi, come per esempio inferiori produzioni di latte o inferiore durata della lattazione e infertilità .
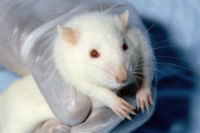 Topi geneticamente modificati possono essere usati per la ricerca sul cancro
Topi geneticamente modificati possono essere usati per la ricerca sul cancro
Modelli per la ricerca su malattie umane . Molte malattie hanno un'origine genetica, o hanno nel genoma fattori predisponenti. Lo studio di alcune malattie può essere estremamente facilitato usando modelli animali sperimentali che riproducano alcuni tratti del genoma umano che sono alla base di alcune patologie. L'uso di animali da laboratorio (specialmente topi e ratti) geneticamente modificati è già diffuso per lo studio di una serie di malattie, principalmente il cancro [14] .
-
Xenotrapianti . Uno dei settori di ricerca delle biotecnologie riguarda lo studio di animali che possano essere donatori di organi per xenotrapianti . Gli xenotrapianti sono trapianti di organi da una specie non umana all'uomo, e potrebbero essere una nuova frontiera, considerando che la disponibilità di organi per gli allotrapianti (da uomo a uomo) è sempre inferiore alle richieste. Il suino è considerato la specie più adatta a questo scopo, perché presenta delle somiglianze dal punto di vista anatomico . Il maggiore ostacolo è tuttavia quello immunologico , cioè che l'organismo ricevente rigetti il trapianto producendo anticorpi contro l'organo trapiantato. In questo senso gli approcci transgenici puntano a inibire le reazioni ancticorpali responsabili del rigetto [15] . Altri studi hanno invece puntato sul trapianto di cellule o tessuti transgenici, che potrebbero offrire interessanti possibilità per la cura di diverse malattie, ad esempio il morbo di Parkinson [16] .
-
Miglioramento delle produzioni animali . Tra le ricerche sulla transgenesi animale, alcune hanno il fine di aumentare la redditività dell'allevamento puntando sulla modificazione genetica volta a migliorare la qualità di alcune produzioni (ad esempio latte, lana), ad aumentare la produzione di carne, la prolificità o la resistenza alle malattie. Un esperimento del 2003 ha dimostrato che è possibile modificare geneticamente le vacche in modo che producano un latte a più alto contenuto in caseina , una proteina importante nel processo di produzione del formaggio [17] . Altri ricercatori hanno studiato, nel topo, la possibilità di produrre un latte a ridotto contenuto in lattosio , che potrebbe essere assunto anche da soggetti intolleranti [18] .
Normativa sugli OGM
(Per approfondire, vedi la voce Normativa sugli OGM)
In molti Paesi del mondo esiste un quadro di riferimento normativo che regola il settore OGM, per garantire la biosicurezza , ossia un utilizzo in rispetto dei necessari livelli di sicurezza ambientale, della salute umana e di quella animale. I principi legislativi di riferimento a livello internazionale in tema di biosicurezza sono contenuti all'interno del Protocollo di Cartagena .
In Europa il contesto normativo sugli OGM, basato sul principio di precauzione , è oggi costituito dai seguenti testi:
-
Direttiva 2001/18/CE [19] , che, sostituendo la 90/220/CEE, riscrive le regole base per l'autorizzazione al rilascio nell'ambiente di un nuovo OGM;
-
Regolamenti 1829 [20] e 1830/2003/CE [21] , che regolano l'autorizzazione e l'etichettatura/tracciabilità degli alimenti e dei mangimi (food & feed) costituiti o derivati da OGM;
-
Raccomandazione 556/2003 [22] , che indica le linee guida sulla coesistenza tra colture OGM e convenzionali, cui le norme nazionali e regionali dovrebbero allinearsi.
L' Italia ha recepito la direttiva 2001/18/CE attraverso il decreto legislativo 224/2003 [23] .
Il dibattito sugli OGM
(Per approfondire, vedi la voce Dibattito sugli OGM)
L'introduzione di organismi geneticamente modificati (in particolare nel settore agroalimentare) ha creato spesso forti attriti all'interno dell'opinione pubblica di molti Paesi. Esiste oggi un intenso dibattito in proposito all'interno della comunità internazionale.
Tra i temi più dibattuti vi sono la legittimità di brevettare organismi viventi,pratica attualmente molto in uso in agricoltura, e le implicazioni etiche legate all'uso di animali ingegnerizzati per fini sperimentali (ad esempio l' oncotopo ), o all'uso di cellule embrionali umane a fini di ricerca (trasformazione, clonazione, chimerizzazione).
I punti maggiormente controversi in relazione all'uso degli OGM in ambito agroalimentare riguardano i potenziali rischi per l'ambiente o per la salute umana e animale, la possibilità di coesistenza tra colture OGM e non-OGM e l'impatto economico-sociale della loro introduzione in aree rurali, soprattutto in Paesi in via di sviluppo.
Voci correlate:
Biotecnologia
-
Ingegneria genetica
-
DNA ricombinante
-
Piante transgeniche
-
Topi transgenici
-
Topi knock-out
-
Rivoluzione verde
-
Diamond contro Chakrabarty
Note
^ Direttiva 2001/18/CE - Allegato I A:TECNICHE
-
^ Morandini Piero, Creso e i suoi fratelli. Tempi num.20 del 24 maggio 2000
-
^ ( EN ) Cohen, S., Chang, A., Boyer, H. & Helling, R. (1973) Construction of Biologically Functional Bacterial Plasmids In Vitro. Proc. Natl. Acad. Sci. USA 70, 3240-3244
-
^ Tappe rilevanti per lo sviluppo della tecnologia del DNA ricombinante
-
^ ( EN ) Berg, P., Baltimore, D., Brenner, S., Roblin, R.O. III, Singer, M.F., "Summary statement of the Asilomar Conference on recombinant DNA molecules," Proc. Nat. Acad. Sci. USA 72, pp. 1981-1984 (1975), also Science 188, p. 991 (1975)
-
^ ( EN ) Sintesi della conferenza di Asilomar
-
^ ( EN ) "Guidelines for research involving recombinant DNA molecules," Federal Register 41, no. 131, pp. 27911-27943 (1976).
-
^ NIH Guidelines for Research Involving Recombinant DNA Molecules
-
^ ( EN ) Genentech: Press Releases - News Release September 6, 1978 The insulin synthesis is the first laboratory production DNA technology
-
^ {en}Wrubel RP, Krimsky S, Anderson MD. Regulatory Oversight of Genetically Engineered Microorganisms: Has Regulation Inhibited Innovation? Environ Manage. 1997 Jul;21(4):571-86. Entrez PubMed 9175544
-
^ ( EN ) L'oncotopo è stato il primo animale GM brevettato
-
^ Jaenisch R, Fan H, Croker B. Infection of preimplantation mouse embryos and of newborn mice with leukemia virus: tissue distribution of viral DNA and RNA and leukemogenesis in the adult animal. Proc Natl Acad Sci U S A. 1975 Oct;72(10):4008-12. Entrez PubMed 1060083
-
^ Melo EO, Canavessi AM, Franco MM, Rumpf R. Animal transgenesis: state of the art and applications. J Appl Genet. 2007;48(1):47-61. Entrez PubMed 17272861
-
^ Marx J. Medicine. Building better mouse models for studying cancer. Science. 2003 Mar 28;299(5615):1972-5. Entrez PubMed 12663895
-
^ Diamond LE, Quinn CM, Martin MJ, Lawson J, Platt JL, Logan JS. A human CD46 transgenic pig model system for the study of discordant xenotransplantation. Transplantation. 2001 Jan 15;71(1):132-42. Entrez PubMed 11211178
-
^ Zawada WM, Cibelli JB, Choi PK, Clarkson ED, Golueke PJ, Witta SE, Bell KP, Kane J, Ponce de Leon FA, Jerry DJ, Robl JM, Freed CR, Stice SL. Somatic cell cloned transgenic bovine neurons for transplantation in parkinsonian rats. Nat Med. 1998 May;4(5):569-74. Entrez PubMed 9585230
-
^ Brophy B, Smolenski G, Wheeler T, Wells D, L'Huillier P, Laible G. Cloned transgenic cattle produce milk with higher levels of beta-casein and kappa-casein. Nat Biotechnol. 2003 Feb;21(2):157-62. Entrez PubMed 12548290
-
^ Stinnakre MG, Vilotte JL, Soulier S, Mercier JC. Creation and phenotypic analysis of alpha-lactalbumin-deficient mice. Proc Natl Acad Sci U S A. 1994 Jul 5;91(14):6544-8. Entrez PubMed 8022817
-
^ Direttiva 2001/18/CE sull'emissione deliberata nell'ambiente di organismi geneticamente modificati e che abroga la direttiva 90/220/CEE
-
^ Regolamento (CE) n. 1829/2003 relativo agli alimenti e ai mangimi geneticamente modificati
-
^ Regolamento (CE) n. 1830/2003 concernente la tracciabilità e l'etichettatura di organismi geneticamente modificati
-
^ Raccomandazione recante orientamenti per lo sviluppo di strategie nazionali e migliori pratiche per garantire la coesistenza tra colture transgeniche, convenzionali e biologiche
-
^ Decreto legislativo 224/2003 - Attuazione della direttiva 2001/18/CE concernente l'emissione deliberata nell'ambiente di organismi geneticamente modificati
Enti
( EN ) Sito della Commissione Europea sugli OGM
-
( EN ) Sito della Biosafety Clearing-House istituita dal Protocollo di Cartagena
-
Sito della Biosafety Clearing-House italiana
Ricerche sugli OGM
( EN ) Sintesi dei risultati dello studio UE sulla sicurezza degli OGM (1985-2000)
-
( EN ) Report FAO su OGM e paesi poveri
Altri approfondimenti
( EN ) GMO Compass, sito di informazione indipendente sugli OGM, finanziato nell'ambito del Sesto Programma Quadro della Commissione Europea
-
Le risposte alle domande più frequenti sugli OGM a cura della Società Italiana di Genetica Agraria
-
Approfondimento sugli OGM a cura dell' Associazione Nazionale Biotecnologi
-
( EN ) Database delle pubblicazioni sulla sicurezza degli OGM dal 1990 ad oggi, a cura dell' International Center for Genetic Engeneering and Biotechnology
-
BiocomMedia, sito indipendente di informazione tecnico-scientifica sugli OGM
-
( EN ) Alcune analisi di approfondimento sull'impatto economico degli OGM sui redditi agricoli, a cura di PG Economics , società inglese di consulenza economica in settore agrario e alimentare